![]()
1 Biologie und Physiologie des Implantatlagers unter Berücksichtigung von Transplantationsverfahren
1.1 Einleitung
Mit der Einführung enossaler Implantate in die Zahnheilkunde wurde dem Behandler die Möglichkeit eröffnet, auch bei Verlust mehrerer, vor allem strategisch wichtiger Zähne festsitzende prothetische Versorgungen durchzuführen und somit herausnehmbaren Ersatz in vielen Fällen zu vermeiden. Doch waren es zunächst die Menge und die Qualität des Knochens, die die vielfältigen Möglichkeiten implantatgetragener Restaurationen einschränkten. Schon sehr früh nach dem Entfernen von Zähnen zeigt sich zunächst ein Verlust der Breite und anschließend auch der Höhe des Alveolarfortsatzes.20,21 Ein Defizit in der horizontalen Relation konnte durch besondere Implantatformen, wie Blatt- oder Klingenimplantate, ausgeglichen werden, deren Möglichkeiten jedoch beschränkt und deren Langzeitprognosen unsicher waren.59,128 In der Folgezeit wurde ein Vielzahl von Verfahren entwickelt, um verlorenen Alveolarknochen zu regenerieren bzw. zu reparieren.23,88 Hierbei zeigte sich, dass das Verständnis der Anatomie und Physiologie des Knochens von entscheidender Bedeutung für den Einsatz und den Erfolg dieser Verfahren war.157 Ziel dieses Kapitels ist eine Darstellung der Grundzüge des Knochenstoffwechsels zum besseren Verständnis der Transplantationsverfahren.
1.2 Die Zellen des Knochenstoffwechsels
Eine Beschränkung der Darstellung des Knochenstoffwechsels auf die beiden Zelllinien der Osteoblasten/ Osteozyten und Osteoklasten kann der Komplexität der Vorgänge, an denen eine Vielzahl von Mediatoren, Hormonen, Zellen und Stoffwechselprodukten beteiligt ist, nicht gerecht werden. Dennoch müssen hier zunächst die beiden wichtigsten Zellgruppen des Knochens beschrieben werden.
1.2.1 Osteoblasten
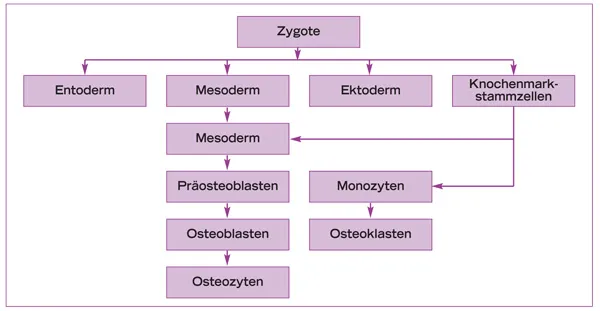
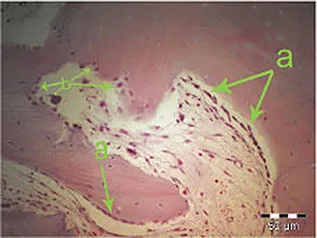
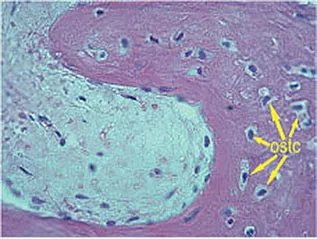
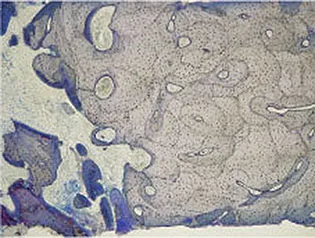
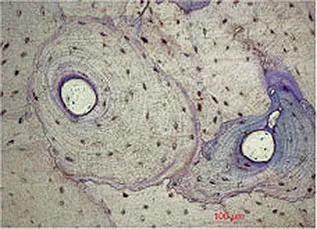
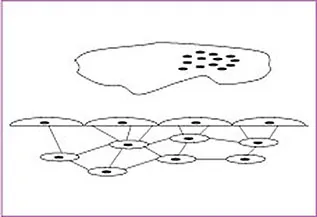
Osteoblasten gehen aus pluripotenten mesenchymalen Vorläuferzellen hervor (Abb.1-1a). Während der Knochenbildung produzieren sie die Knochenmatrix, aus der durch Mineralisationsvorgänge die Hartsubstanz entsteht. Im Verlauf der Knochenumbauvorgänge werden die Osteoblasten (Abb.1-1b,c) in die Knochenmatrix eingemauert und entwickeln sich zu metabolisch wenig aktiven Osteozyten (Abb.1-1d). Als solche liegen sie jedoch nicht auf Diffusion angewiesen ruhend im Knochen, sondern kontrollieren über Gap junctions der zytoplasmatischen Fortsätze den Ionentransport. Dieser ist ein unentbehrlicher Faktor für die Knochenernährung und diverse Austauschvorgänge, da ein reiner Diffusionsaustausch durch die mineralisierte Matrix eigentlich nicht möglich ist. Die Einschränkung des Ionentransports auf ca. 100µm bewirkt die Beschränkung der Größe von Osteonen auf eben diese Strecke.46 Somit bilden Osteone nicht nur eine strukturelle, sondern auch eine metabolische Einheit (Abb.1-1e, f).
Abb. 1-1a Differenzierung von Osteoblasten und Osteoklasten (nach Nefussi 200799).
Abb. 1-1b Typische Osteoblasten über einer neu gebildeten Osteoidschicht (Färbung: Masson-Trichrom).
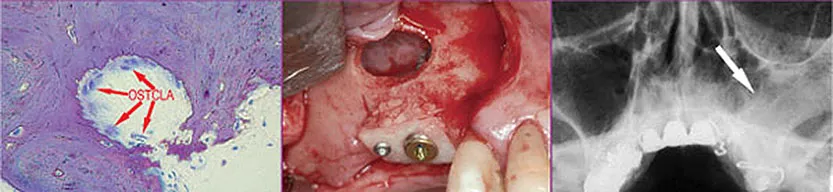
Abb. 1-1c (a) Osteoblastenschichten, (b) Osteoklasten.
Abb. 1-1d Multiple, vitale Osteozyten (Färbung: Toluidinblau, basisches Fuchsin).
Abb. 1-1e Multiple Osteone: Die Osteozyten sind in einem sehr dichten Havers’schen System eingemauert. Durch die Knochenneubildung verkleinert sich im Laufe der Zeit das Lumen der Havers-Kanäle (Färbung: Thioninblau).
Abb. 1-1f Vergrößerter Ausschnitt aus Abbildung 1-1e.
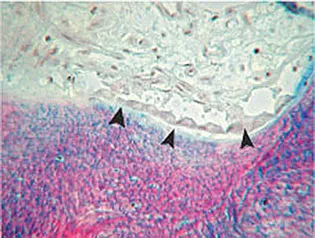
Auf der Oberfläche des Knochens liegende abgeflachte Osteoblasten werden auch „ruhende Osteoblasten“ oder „Bone lining cells“ genannt (Abb.1-2a). Ihnen werden neben einer Mitwirkung an der metabolischen Aktivität des Knochens auch eine Barrierefunktion und die Kontrolle des Ionenflusses zwischen diesem und dem extraossären Raum zugeschrieben. Zudem spielen sie eine Rolle bei der Regulierung des Knochenabbaus, indem sie Mediatoren freisetzen, die durch Kontraktion der ruhenden Grenzzellen die Oberfläche für die Osteoklasten frei machen und diese selbst zur Resorption aktivieren (Abb.1-2a).58
Abb. 1-2a Darstellung einer metabolischen Knocheneinheit: Die Bone lining cells der Knochenoberfläche stehen mit den Osteoblasten in Verbindung. Osteoklasten können an der Knochenoberfläche nicht wirksam werden, solange die Bone lining cells die Oberfläche nicht freimachen (nach Martin 200884).
1.2.2 Osteoklasten
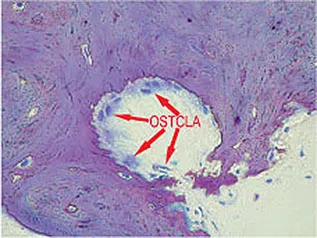
Im Gegensatz zu den Osteoblasten stammen die Osteoklasten nicht von mesenchymalen, sondern von hämatopoetischen Stammzellen ab.137 Besonders wahrscheinlich scheint eine Herkunft von Granulozyten-Makrophagen-Vorläuferzellen.70,85 Die Osteoklasten bilden eine Gruppe von auf den Abbau kalzifizierter Gewebe spezialisierten Riesenzellen (Abb. 1-2b). Sie finden sich in den sogenannten Howship-Lakunen, Resorptionslakunen im Hartgewebe, und zeigen eine positive Saure-Phosphatase-Reaktion.22,95 Bei einer Zellgröße zwischen 30 und 100µm weisen sie eine Anzahl von ca. 3 bis 30 Kernen auf (Abb. 1-2c). Im acidophilen Zytoplasma zeigen sich Vakuolen, die auf den aktiven Abbauprozess hinweisen.
Abb. 1-2b Osteoklasten neben resorbiertem Knochen.
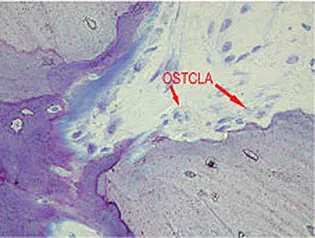
Abb. 1-2c Osteoklasten mit multiplen Nukleonen (Histologie der Abbildungen 1-1e bis 1-1f sowie 1-2b und 1-2c: Dr. D. Moser und Prof. Dr. Dr. R. Ewers, Universität Wien).
Das marginale Areal des Osteoklasten, die klare Zone, befindet sich in Nachbarschaft zum kalzifizierten Gewebe.50 Der zentrale Anteil der Riesenzelle zeigt eine Vergrößerung der Zelloberfläche, das sogenannte „Ruffled border“, das durch Einstülpungen der Zellmembran entsteht. An dieser vergrößerten Oberfläche werden Protonen freigesetzt, die den pH-Wert senken und so die Hartsubstanzen auflösen. Die nach der Auflösung des Hydroxylapatits freiliegenden Kollagenfasern werden anschließend durch lysosomale Enzyme und Kollagenasen abgebaut.147
Für Osteoklasten wurden zwei unterschiedliche Differenzierungswege identifiziert: Der eine ist abhängig von einer Interaktion mit Osteoblasten und erklärt den Wechselprozess von Knochenabbau und -aufbau, der während der physiologischen Knochen-remodellierung stattfindet. Der zweite Weg wird durch Zytokine gesteuert, die während einer Entzündung oder eines Traumas freigesetzt werden, und steht mit dem Knochenverlust bei pathologischen Ereignissen in Zusammenhang. Von den Entzündungsmediatoren sind als besonders relevant für den dentalen Bereich das Interleukin-1 (IL-1) und der Tumor necrosis factor-α (TNF-α) zu nennen.8,56,68 Untersuchungen der letzten Jahre konnten zeigen, dass einige Menschen mit einer verstärkten Freisetzung dieser Mediatoren und somit einem erhöhten Knochenabbau auf entzündliche Reize reagieren.10,69
1.3 Die Kaskade des Knochenumbaus
Die Genetik und Entwicklungsbiologie des Knochenauf- und umbaus wird von Nefussi zu drei wesentlichen Schritten zusammengefasst:61–63,99,153
-
Am Anfang steht die als zelluläre Kondensation bezeichnete Ansammlung und Reifung zellulärer Massen, die den Ursprung des skelettalen Musters bildet.
-
Nachdem die Kondensation erfolgreich abgeschlossen wurde, ist der zweite Schritt die Aktivierung und Regulation von Genen, die für die zelluläre Differenzierung verantwortlich sind.
-
Im letzten Schritt erfolgt die Aktivierung von Genen, die den Prozess der Matrixsynthese und -mineralisierung, die hormonale Aktivität sowie die Adaptation an Strain und Stress durch Remodellierung steuern.
Alle drei Schritte laufen unter Vermittelung durch spezifische Transkriptionsfaktoren ab, die bestimmte Gene aktivieren oder abschalten. Auch nach Abschluss des Knochenwachstums können im Rahmen der Knochenheilung einige dieser Mechanismen aktiviert werden.9,24,39,41,42,152
1.3.1 Zelluläre Kondensation
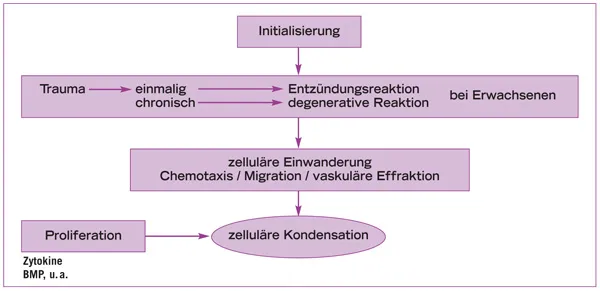
Der Begriff der zellulären Kondensation bezeichnet eine durch ortsabhängige Transkriptions- und Wachstumsfaktoren induzierte Ansammlung von Zellen zu einer Masse, die die Quelle für die Reparatur des Knochendefekts darstellt. Sie wird durch traumatische Ereignisse jeglicher Form ausgelöst und führt entweder zu einer Entzündung oder zur Degeneration (Abb.1-3). Da die Zellmasse die Quelle für die Reparatur des Knochendefekts darstellt, ist der erfolgreiche Abschluss der Regeneration von der Potenz und Größe der Agglomeration abhängig. Es kann also zu einer Diskrepanz zwischen der Potenz der Zellmasse und dem Ausmaß des zu reparierenden Defektes kommen, die einen Knochenverlust nach sich zieht.
Abb. 1-3 Hauptschritte der zellulären Kondensation (nach Nefussi 200799).
1.3.2 Zelluläre Differenzierung
Im zweiten Schritt beeinflussen lokale, ortsspezifische Signalmoleküle der Zellkondensation zelluläre und ZellMatrix-Interaktionen und bewirken die osteogenetische Differenzierung der Zellmassen. Die Zelldifferenzierung bedeutet für die Zelle die endgültige Reifung und führt zu voller Funktionalität. Durch sie entstehen die oben beschriebenen Zelltypen der Osteoblasten/Osteozyten und Osteoklasten.
1.3.3 Matrixsynthese und -mineralisation
Die Osteoblasten synthetisieren im wachsenden oder heilenden Knochen Kollagen, Proteoglykane und Glykoproteine, die im Extrazellularraum eine spezifische Quartärstruktur bilden. An dieser Matrix vollzieht sich der Mineralisationsvorgang. Zunächst beginnen die Osteozyten mit der intrazellulären Akkumulation von Kalzium und Phosphat in spezifischen Sekretions-vesikeln, die anschließend aktiv aus der Zelle ausgeschleust werden. Sie enthalten außerdem alkalische Phosphatase. In den Vesikeln bilden sich Apatitkristalle, die sich nach deren Auflösung an den extrazellulären Nukleationsorten (bevorzugt Kollagenfasern und knochenspezifische kalziumbindende Proteine) anlagern.43 In der Mineralisationszone findet sich eine erhöhte Aktivität der alkalischen Phosphatase. Das Fehlen dieses Enzyms ist durch defekte Knochenbildung gekennzeichnet. Nach Abschluss der Mineralisation besteht Knochen zu ca. 65 % aus anorganischer Substanz, hauptsächlich Hydroxylapatit, aber auch Magnesium, Kalium, Chlor, Eisen und Karbonat, sowie zu 25 % aus organischer Substanz und zu 10 % aus Wasser. Die organische Matrix setzt sich aus Kollagen Typ I (90 %) sowie nichtkollagenen Proteinen (z.B. Osteonektin, Osteocalcin, Sialoprotein u.a...