![]()
scappamento
vedi: battito di scappamento
scompenso cardiaco e aritmie. Lo scompenso cardiaco può essere considerato la via finale comune di situazioni anche estremamente differenti, accomunate dalla presenza di una disfunzione ventricolare (sistolica e/o diastolica), che dà luogo all’attivazione di una serie di meccanismi sistemici/neuroendocrini, i quali se da un lato attenuano le conseguenze deleterie della disfunzione ventricolare, dall’altro producono effetti miocardiotossici, portando in definitiva a rimodellamento ventricolare sfavorevole, perdita di cellule (apoptosi; necrosi cellulare “attiva”), aritmie. Tutto ciò aggrava ulteriormente la disfunzione ventricolare, dando luogo ad un circolo vizioso che porta alla sindrome clinica dello scompenso cardiaco. I pazienti con scompenso cadiaco muoiono per due ragioni: deficit circolatorio o morte improvvisa. Se nel secondo caso un legame diretto tra aritmie e prognosi dello scompenso è fin troppo evidente, non va trascurato il ruolo che le aritmie hanno nel peggiorare lo scompenso, in una sorta di circolo vizioso che pone le aritmie, anche sopraventricolari, come effetto e causa dello scompenso. Tra le aritmie sostenute associate a scompenso cardiaco, la fibrillazione atriale è di gran lunga la più frequente e la prevalenza è in rapporto al grado di compromissione funzionale. Così, nella classe funzionale NYHA I la prevalenza è attorno al 5%, mentre nella classe IV la prevalenza sfiora il 50%. Questa forte tendenza da parte dello scompenso cardiaco a determinare l’insorgere di fibrillazione atriale, ha svariate motivazioni:
>
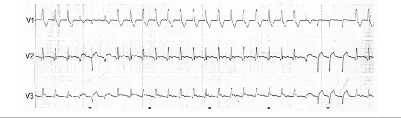
Figura 66. Uomo di 56 anni, ricoverato in UTIC per STEMI anteriore. Tracciato registrato a 5 ore dall’ingresso, dopo terapia trombolitica. Il tracciato mostra ritmo sinusale interrotto da fasi di ritmo idioventricolare accelerato. Evidenti battiti di fusione. Questo disturbo del ritmo, in questa situazione clinica, viene ritenuto un marker elettrico di avvenuta riperfusione.
>
a) dilatazione atriale: nella maggioranza dei casi di scompenso cardiaco esiste dilatazione di una o di entrambe le camere atriali, con prevalenza di quella sinistra. La dilatazione atriale modifica il substrato in senso più propizio all’insorgere di fibrillazione atriale in quanto si accompagna ad aumento della massa critica, con conseguente incremento, anche per una ragione puramente geometrica, dello spazio disponibile per rientri multipli. Sono state inoltre dimostrate alterazioni delle correnti ioniche di membrana in atri umani dilatati che possono giustificare il netto incremento della vulnerabilità atriale;
b) stretch atriale: Il sovraccarico di pressione e di volume che si verifica nelle camere atriali in corso di scompenso cardiaco induce uno stiramento cronico più o meno importante delle fibrocellule atriali. Tale “stretch” ha una serie di effetti, gran parte dei quali orientati nettamente nel favorire l’insorgere ed il perpetuarsi della fibrillazione atriale. Esso favorisce la comparsa di automatismo patologico “triggerato” da post-potenziali tardivi con facile comparsa, nell’ambito della muscolatura atriale, di foci ectopici che fungono da trigger di fibrillazione atriale. Lo stretch atriale si accompagna a riduzione della velocità di conduzione il che rende il substrato atriale più propizio a fenomeni di rientro. Peraltro, gli effetti elettrofisiologici dello stretch sono disomogenei e ciò accentua il fenomeno dell’anisotropia non uniforme, e quindi la propensione al rientro;
c) attivazione neuro-ormonale: l’attivazione ortosimpatica tipica dello scompenso incrementa l’attività di foci ectopici e accorcia i periodi refrattari, entrambi effetti che favoriscono l’insorgere di fibrillazione atriale. È stato inoltre dimostrato recentemente, sia in modelli animali che nell’uomo, che nello scompenso cardiaco, oltre ad un aumento del tono simpatico, si verifica una riduzione del tono parasimpatico. Un’alterata attività parasimpatica, in combinazione con un’iperattività ortosimpatica, potrebbe avere un ruolo importante nell’insorgere di tachiaritmie, ventricolari e sopraventricolari. L’attivazione del sistema renina-angiotensina-aldosterone influenza la sintesi e la degradazione della matrice extracellulare, favorendo – attraverso un incremento di angiotensina II – la fibrosi interstiziale. La fibrosi amplifica la disomogeneità delle proprietà elettrofisiologiche delle fibrocellule atriali, in termini di durata dei periodi refrattari e di velocità di conduzione, il che accentua l’anisotropia non uniforme e quindi la propensione da parte del substrato atriale ad andare incontro a fibrillazione;
d) rimodellamento dei canali ionici: lo scompenso indotto sperimentalmente nell’animale con pacing ad elevata frequenza causa rimodellamento dei canali ionici nell’ambito del tessuto atriale, che coinvolge diverse correnti di membrana. Probabilmente, il fenomeno ionico più importante è il sostanziale incremento della corrente di scambio Na+/Ca++ osservata nelle fibrocellule atriali, che può portare a comparsa di post-potenziali tardivi e conseguentemente ad attività “triggered”. Quest’ ultima aumenta il “burden” di battiti atriali ectopici, che possono fungere da trigger di fibrillazione atriale. Altre modificazioni ioniche tipiche dello scompenso includono una ridotta “L-type Ca++ current” e una riduzione delle correnti del potassio, che possono avere conseguenze sulla refrattarietà atriale, l’automatismo atriale, la velocità di conduzione;
e) Modifiche della matrice extracellulare: solo recentemente è stata messa nella giusta evidenza l’importanza della matrice extracellulare da un punto di vista aritmologico. La matrice extracellulare non solo fornisce supporto strutturale ai miociti e garantisce l’integrità architettonica e la geometria del tessuto, ma interagisce con gli stessi miociti nel processo della conduzione. È dimostrato che l’omogeneità della conduzione dell’impulso nell’ambito della muscolatura atriale si basa non solo sull’integrità e l’interazione tra i miociti, ma anche sulla natura della matrice extracellulare che è attorno ai miociti. In modelli sperimentali di scompenso cardiaco è possibile indurre facilmente fibrillazione atriale anche senza nessuna alterazione di proprietà elettrofisiologiche delle cellule, a patto che vi sia un’estesa fibrosi interstiziale dell’atrio. La fibrosi interstiziale facilita l’insorgenza di blocchi di conduzione locali che incrementano la propensione al rientro. Va dunque sottolineata una stretta interconnessione fisiopatologica tra fibrillazione atriale e scompenso cardiaco, una sorta di intreccio assimilabile ad un vero e proprio circolo vizioso nel quale è spesso difficile individuare nel singolo caso il punto di partenza.
I soggetti con scompenso cardiaco hanno un rischio di morte improvvisa pari a 6-9 volte quello della popolazione generale.La morte improvvisa è in questo contesto un’espressione fenotipica piuttosto complessa, che risulta dall’interazione di una serie di fattori. Tra questi:
a) il substrato, comprendente un miocardio più o meno alterato, diffusamente o distrettualmente, con relativo rimodellamento delle proprietà di membrana, attive e passive connesse ad alterazioni più o meno cospicue delle correnti ioniche trans-membrana;
b) fattori funzionali di diverso genere, neuroendocrini, farmacologici, elettrolitici, ischemici (ischemia miocardica acuta, riperfusione, ischemia “cronica”) che modulano il substrato in modo più o meno propizio all’innesco di aritmie maligne;
c) fattori trigger intercorrenti, rappresentati in genere da ectopie ventricolari;
d) una predisposizione genetica all’instabilità elettrica che porta alla morte improvvisa. Il rischio di morte improvvisa nello scompenso è dinamico e fluttuante, varia nel tempo, con il mutare delle diverse variabili coinvolte nell’evento: questo fa della stratificazione prognostica un problema complicatissimo, che pare oggi sminuire il ruolo esclusivo della frazione d’eiezione valutata all’ecocardiogramma come snodo decisionale ai fini dell’impianto di ICD in prevenzione primaria. Peraltro, in tale contesto, non è trascurabile il meccanismo bradiaritmico e la dissociazione elettromeccanica come causa di morte improvvisa. Non va comunque trascurato il fatto che nelle ultime due decadi si assiste ad un netto declino dell’incidenza di morte improvvisa nello scompenso cardiaco, probabilmente in relazione al vasto impiego di farmaci che indirettamente (ma nettamente) influenzano l’aritmogenenesi, come gli ACE inibitori, i beta boccanti, i sartanici, il secubitril, gli antialdosteronici.
segnapassi
vedi: pacemaker
segnapassi migrante. Sinonimo di “wandering pacemaker”. Consiste nel mutamento continuo della sede di insorgenza dell’impulso, nell’ambito del nodo del seno, dell’atrio, della giunzione AV, con conseguenti continue variazioni della morfologia dell’onda P, del ciclo PP, dell’intervallo PR.
seno coronarico. Le vene cardiache confluiscono nel seno coronarico, che decorre nel solco atrio-ventricolare sinistro parallelamente all’arteria coronarica circonflessa fino a portarsi anteriormente e sboccare nell’atrio di destra, inferiormente al triangolo di Koch (vedi triangolo di Koch). All’ostio, sono talora presenti le vestigia di una valvola, la valvola di Tebesio. L’incannulamento del seno coronarico ha una cruciale importanza in elettrofisiologia per varie ragioni:
1. al suo interno, vengono posizionati elettrocateteri durante studio elettrofisiologico per mappare la sede di vie accessorie atrio-ventricolari, per altri tipi di mappaggio e per la stimolazione atriale sinistra;
2. al suo interno e nei suoi rami distali vengono inseriti gli elettrocateteri utilizzati per la stimolazione del ventricolo sinistro nella terapia di resinconizzazione cardiaca (stimolazione biventricolare);
3. dal seno coronario possono essere effettuate procedure interventistiche-ablative;
4. funge da repere anatomico per la puntura del setto interatriale.
sensing
vedi: pacemaker
SIDS. È l’acronimo di Sudden Infant Death Syndrome, con il quale universalmente viene indicata la morte improvvisa infantile. Più precisamente, il termine definisce il verificarsi di un evento mortale improvviso e inspiegato entro il primo anno di vita in un bambino ritenuto perfettamente sano, e nel quale né l’indagine autoptica né lo studio delle circostanze di morte, né la storia clinica, inclusa quella familiare, forniscono elementi certi sulle cause dell’evento fatale. Fattori di rischio per SIDS sono comunemente ritenuti: la prematurità, il dormire in posizione prona (“sullo stomaco”) o su un lato, il surriscaldamento, l’esposizione al fumo di tabacco, il potenziale rischio di soffocamento accidentale durante la condivisione del letto con i genitori, il potenziale rischio di soffocamento da oggetti morbidi, le infezioni, la tossicodipendenza dei genitori. In rari casi, l’infanticidio sotto forma di soffocamento intenzionale può essere erroneamente diagnosticato come SIDS. Non esistono ad oggi certezze quanto alla patogenesi della SIDS, e probabilmente la via patogenetica non è univoca. Le ipotesi sinora formulate sembrano delineare un quadro multifattoriale, nel quale diversi fattori di rischio, insufficienti se presi singolarmente, possono cooperare creando una condizione propizia al drammatico evento. Si è così fatta strada la cosiddetta ipotesi del triplo rischio, in base alla quale una supposta vulnerabilità intrinseca del bimbo si interseca con fattori esogeni e con un peculiare momento biologico intrinseco relativo al momento in cui l’evento si verifica. Il concetto di vulnerabilità intrinseca ha assunto nel corso degli anni i connotati di suscettibilità genetica e in tale ambito la ricerca ha spaziato prendendo in considerazione diversi aspetti genetici, attinenti ad ambiti immunitari, neuro-modulatori, enzimatici e relativi alle canalopatie genetiche. In questo senso, uno storico studio di PJ Schwartz comparso nel nel 1998 sul New England Journal of Medicine, già dimostrava in modo inequivocabile che un allungamento dell’intervallo QT nella prima settimana di vita costituisce un importante fattore di rischio per la SIDS. Successive ricerche dello stesso gruppo hanno fornito ulteriori dimostrazioni del collegamento molecolare tra SIDS e LQTS, con ciò ribadendo l’importanza di uno screening elettrocardiografico neonatale, che potrebbe contribuire al riconoscimento precoce di alcune delle possibili future vittime di SIDS. Vi sono peraltro evidenze di casi di SIDS nei quali sono state dimostrate all’indagine “autoptica mecolare” la presenza di mutazioni tipiche della sindrome di Brugada, della tachicardia ventricolare polimorfa catecolaminergica, della sindrome del QT corto, sebbene la loro incidenza sia nettamente inferiore rispetto all’associazione con la sindrome del QT lungo.
signal averaging. Tecnica di registrazione dell’ECG che consente di rilevare segnali elettrici di piccolissima ampiezza direttamente dalla superficie corporea. Consiste nel registrare molti segnali elettrocardiografici consecutivi, amplificarli e sovrapporli, eseguendo una media, in modo da elidere il rumore di fondo, che è casuale, utilizzando solo i segnali che possiedono un rapporto temporale costante con un punto di riferimento. È possibile in questo modo registrare il potenziale del fascio di His ed eventuali potenziali tardivi.
sincope. Il termine (dal greco “synkoptein”, spezzare, stroncare) indica una brusca sospensione dell’attività vitale ed è utilizzato per indicare un’improvvisa e transitoria perdita dello stato di coscienza e del tono posturale. Nella massima parte dei casi consegue ad una riduzione critica del metabolismo cerebrale, per lo più secondaria ad un’improvvisa ipossia cerebrale. L’ipossia a sua volta può derivare:
a) da una brusca caduta della pressione di perfusione cerebrale (da ipotensione arteriosa sistemica o da riduzione locale di flusso);
b) da una critica caduta della portata cardiaca (o da una sua inadeguata distribuzione);
c) da ipossiemia arteriosa acuta o comunque da alterata composizione del sangue;
d) da più di queste cause in associazione.
Una distinzione eziologica può essere fatta tra sincopi da causa non cardiaca e sincopi da causa cardiaca. Tra le prime, le sincopi neuromediate sono probabilmente le più frequenti (vedi: sincope neuromediata). Altri tipi di sincope non cardiogena sono: sincopi neurovascolari, sincopi da deficit del ritorno venoso, sincopi da cause metaboliche, sincopi ipossiemiche, sincopi da cause farmacologiche (o tossiche in generale), sincopi psicogene (iperventilazione, isteria).
Nelle sincopi cardiogene, la deficiente perfusione cerebrale alla base del disturbo riconosce una genesi cardiaca. Vediamo le varie cause possibili di sincope cardiogena:
1. ostacolo (fisso o dinamico) all’eiezione ventricolare sinistra (stenosi aortica, cardiomiopatia ipertrofica, tumori endocavitari del ventricolo sinistro);
2. ostacolo al riempimento di entrambi i ventricoli (tamponamento cardiaco) o di uno di essi (trombo atriale a palla; stenosi mitralica serrata; tumore cardiaco);
3. improvviso ostacolo all’efflusso ventricolare destro, come nell’embolia polmonare;
4. deficit acuto della funzione contrattile (infarto miocardico acuto esteso; spasmo coronarico multivasale; stadi terminali delle cardiomiopatie dilatative);
5. aritmie. Una sincope causata da un evento aritmico si identifica con la cosiddetta “sindrome di Morgagni-Adams-Stokes” (vedi questa voce). Variazioni critiche di frequenza cardiaca (sia riduzioni che aumenti) si traducono, al di là di un certo limite, in una riduzione di portata cardiaca che può portare a sincope. Tale limite non è fisso, ma viene condizionato fortemente dalla situazione cardiaca di base del soggetto e da fattori concomitanti (neurovegetativi, circolatori locali e sistemici, ecc.). Disturbi del ritmo potenzialmente sincopali sono:
- malattia del nodo del seno;
- disturbi della conduzione;
- tachiaritmie sopraventricolari;
- tachiaritmie ventricolari.
sincope neuromediata. Con questa denominazione generica vengono indicate una serie di situazioni sincopali prodotte da meccanismi riflessi, che in definitiva sfociano in una inappropriata vasodilatazione (con evidente maldistribuzione della portata cardiaca) e/o in bradicardia più o meno...