La sempre maggiore attenzione alla spesa sanitaria, con il verticale aumento della domanda, le conseguenti misure restrittive e la necessità di allocare risorse nel modo più efficiente impongono di assegnare il giusto valore al farmaco nel prezzo e nella rimborsabilità, in termini assoluti e di confronto con farmaci simili di analogo profilo o verso altre prestazioni sanitarie alternative. Nel corso degli ultimi anni sono state sviluppate e affinate numerose tecniche e metodologie per identificare quale tra i farmaci utilizzabili in alternativa per una specifica indicazione e patologia ha il migliore rapporto tra costi che richiede e risultato per il paziente.Ecco allora la farmacoeconomia, insieme di strumenti indispensabili per misurare quanto vale un farmaco in rapporto ai benefici che offre, sia in senso assoluto sia in confronto ai competitori.Questo volume intende fornire gli strumenti di realizzazione, valutazione e interpretazione di ricerche farmacoeconomiche.

- 192 pages
- English
- ePUB (mobile friendly)
- Available on iOS & Android
eBook - ePub
About this book
Trusted by 375,005 students
Access to over 1.5 million titles for a fair monthly price.
Study more efficiently using our study tools.
Information
Capitolo 1
Market access


Lo stato si propone di assicurare un’adeguata assistenza sanitaria con infrastrutture e servizi attuando scelte economiche per uno sviluppo equilibrato ed equo di ogni settore della sanità.
Nell’ultimo cinquantennio l’evoluzione dei sistemi di sanità ha seguito tre fasi principali (figura 1.1) in relazione all’espansione della domanda e dell’offerta; fasi dettate dalle risorse disponibili e modulate sulla sostenibilità economica dell’evoluzione della domanda determinata dalle variabili demografiche.
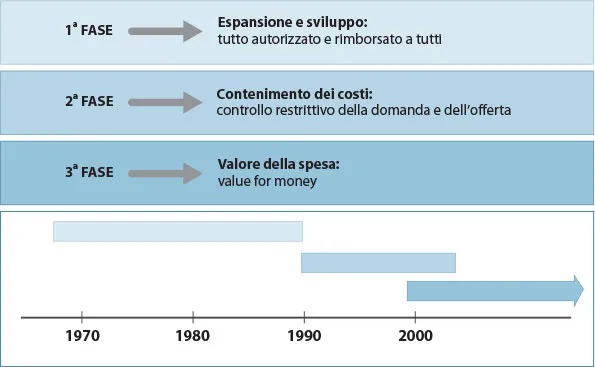
Figura 1.1 Fasi evolutive dello sviluppo dei sistemi sanitari. (Fonte: Gianfrate, 2013)
Oggi siamo in una fase avanzata di richiesta di dimostrazione del valore delle prestazioni e dei farmaci pagati dal Servizio sanitario nazionale (SSN).

I farmaci, benché assorbano solo una quota all’incirca del 16% della spesa sanitaria pubblica, costituiscono il presidio terapeutico più utilizzato e quindi maggiormente soggetto alle dinamiche demografiche di invecchiamento, cronicizzazione delle malattie e desiderio di benessere.
La principale criticità dei farmaci è la compatibilità tra spesa pubblica per l’assistenza farmaceutica di qualità, equità nell’accesso senza discriminanti per ogni assistito e remunerazione per l’industria che li scopre e li produce.
In tali compatibilità e sostenibilità, insieme alla possibilità di applicare industrialmente le nuove conoscenze scientifiche, sono racchiuse le specificità del farmaceutico
Nella logica di contenimento della spesa pubblica, la spesa farmaceutica risulta finanziariamente più facile da comprimere rispetto ad altre voci con componenti strutturali e infrastrutturali sulle quali è più difficoltoso intervenire restrittivamente (spesa ospedaliera, personale dipendente ecc.). Le misure di contenimento della spesa farmaceutica riguardano in genere sia la domanda sia l’offerta.
La domanda viene contenuta prevalentemente attraverso una compartecipazione alla spesa del privato (ticket) o vincolando le prescrizioni a determinate patologie e/o pazienti tramite note restrittive (note AIFA) alle prescrizioni stesse e interventi sulle esenzioni per età, reddito e patologia.
Il controllo della domanda mira a ridurre la spesa anche attraverso la correzione dei comportamenti prescrittivi dei medici, in modo che la scelta di una terapia al posto di un’altra tenga conto anche dell’impatto sulla spesa pubblica. Il controllo delle prescrizioni può avvenire in quattro modi:
–limitando il budget massimo di spesa del singolo medico;
–attraverso controlli periodici e limitazioni delle prescrizioni;
–attraverso linee guida prescrittive;
–incentivando l’uso dei generici.
La prima misura è adottata per lo più in Germania e nel Regno Unito, dove vige la libertà di prezzo, perciò si va a incidere più sulla domanda che sull’offerta.
Il controllo delle prescrizioni è invece un iter consolidato in quasi tutti i paesi europei, ma essendo la libertà di prescrizione un valore difeso dai medici, in genere si preferisce intervenire a monte sul numero di confezioni per ricetta e di prescrizioni emesse.
Sta crescendo l’interesse per la terza misura, le linee guida, forme di controllo che suggeriscono gli iter terapeutici e prescrittivi. Le linee guida sono formulate da esperti appartenenti allo stesso mondo medico.
Gli interventi più significativi ed efficaci si concentrano sull’offerta, riducendo i prontuari e i prezzi pagati dal SSN a produttori e distributori. In Italia ciò avviene in modo diretto e indiretto con decreti di taglio, revisione dei prontuari, spostamento dei farmaci nella fascia di non rimborsabilità, imponendo sconti ai produttori e ai distributori, intervenendo sulla distribuzione, imponendo budget a vari livelli con restituzione degli importi che superano i tetti definiti, o pay back, con forme di negoziazione atipiche come il risk sharing, il payment by result ecc.
Queste misure hanno un forte effetto contenitivo sulla spesa SSN ma gravano pesantemente sulla filiera, incidendo negativamente sul conto economico delle aziende, dei distributori, delle farmacie e dell’indotto.
Tra i principali interventi normativi di controllo della spesa farmaceutica SSN dal 2001 si ricordano:
–tagli ripetuti del prezzo per decreto;
–riduzione del CPC;
–nuovo prontuario con prezzo per ATC;
–extra sconti della distribuzione;
–distribuzione diretta e per conto e PHT;
–tetti di spesa, budget aziendali, pay back.
Vale la pena evidenziare, tra le principali misure adottate, l’istituzione di tetti per la spesa convenzionata e quella ospedaliera e di tetti di fatturato per le singole aziende e il singolo prodotto immesso in commercio, che associati al conseguente pay back in caso di sforamento disegnano un meccanismo autoregolato a rimanere nei budget di spesa pubblici previsti. Va ricordato a tale proposito che il pay back, non avendo misure parallele di contenimento della domanda/prescrizione, porta al pagamento da parte delle imprese di un certo numero di trattamenti di pazienti.
Analogamente la distribuzione diretta e per conto, insieme agli sconti obbligatori imposti alla distribuzione, ha pesantemente gravato sui conti delle farmacie.

Nel processo di introduzione di un nuovo farmaco sul mercato, tradizionalmente le dimostrazioni che il titolare del brevetto deve fornire alle autorità preposte alle decisioni di accesso al mercato erano di carattere scientifico-clinico. Nell’ormai cronico contesto di controllo e restrizione della spesa pubblica, alla dimostrazione del plusvalore clinico-medico si è aggiunta la richiesta di valutazione del valore economico del “beneficio” che il nuovo farmaco può apportare, ovvero il value for money, il valore farmacoeconomico (figura 1.2).
L’ottimizzazione del rapporto tra costi e risultati deve tenere in considerazione la prospettiva dell’ambito del processo regolatorio o decisionale, sia esso macro o micro, a cui tale rapporto si applica.
Nella fase iniziale, gli attori principali sono le autorità regolatorie, coinvolte nelle decisioni generali che influenzano sia l’accessibilità ai farmaci (prezzo e rimborsabilità), sia l’uso appropriato degli stessi. Successivamente, durante il processo di regolamentazione, sono coinvolti nelle decisioni anche gli altri attori del sistema di assistenza sanitaria (ad esempio le regioni, i singoli e le unità sanitarie locali, con i rispettivi prontuari locali e ospedalieri o linee guida prescrittive), fino alla fase finale rappresentata da una prescrizione medica per il paziente.
Analizziamo queste fasi a partire dall’esito della ricerca clinica, quando con il dossier registrativo l’azienda titolare del brevetto è pronta a richiedere alle autorità competenti di accedere al mercato.
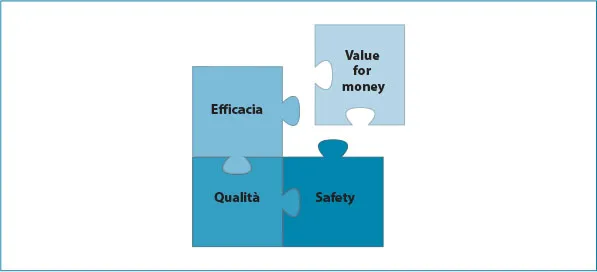
Figura 1.2 Value for money. (Fonte: Gianfrate, 2013)

Completato lo sviluppo di fase III, l’impresa raccoglie tutti i dati prodotti fino a quel momento in un dossier da sottoporre alle autorità per la revisione, prima della concessione dell’autorizzazione all’immissione in commercio. Anche la compilazione di questi documenti è generalmente sottoposta a norme che ne regolano i contenuti e la forma. L’analisi del dossier registrativo è una fase importante sia per l’intero processo di sviluppo sia per i tempi di valutazione della documentazione, che rallentano la registrazione del farmaco.
Le tipologie di autorizzazione sono europee (centralizzata, mutuo riconoscimento, decentrata) o nazionali per alcuni casi specifici (figura 1.3).
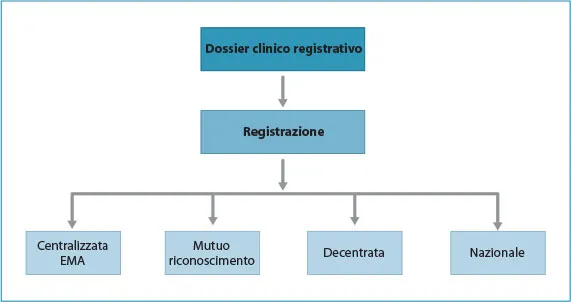
Figura 1.3 Tipologie di autorizzazione all’immissione in commercio. (Fonte: Gianfrate, 2014)
Il carattere vincolante delle procedure di autorizzazione comunitarie è limitato alla registrazione del farmaco e non riguarda la rimborsabilità, materia delle singole autorità nazionali. Le due agenzie preposte a concedere l’autorizzazione all’immissione in commercio (AIC) di un nuovo farmaco o di modifiche a un farmaco sono l’Agenzia Europea per i Medicinali (EMA, European Medicines Agency), per l’intera Unione Europea, e l’Agenzia Italiana del Farmaco (AIFA), con prevalenti responsabilità di attribuzione del prezzo e rimborsabilità da parte del nostro Servizio sanitario nazionale.
L’E...
Table of contents
- Copertina
- Prefazione
- Capitolo 1 – Market access
- Capitolo 2 – Health technology assessment (HTA)
- Capitolo 3 – La valutazione farmacoeconomica
- Capitolo 4 – Costi ed esiti
- Capitolo 5 – Analisi cost of illness (COI)
- Capitolo 6 – Analisi costo-efficacia (CEA)
- Capitolo 7 – Analisi costo-utilità (CUA)
- Capitolo 8 – Valorizzazione e monetizzazione dell’utilità
- Capitolo 9 – CMA, CBA, analisi multiattributo e BIA
- Capitolo 10 – Metodologia e analisi
- Capitolo 11 – La farmacoeconomia nei vari paesi
- Capitolo 12 – L’outcome research
- Capitolo 13 – La comunicazione del valore farmacoeconomico di un farmaco
- Capitolo 14 – Relazioni tra economia, salute e felicità
- Bibliografia
Frequently asked questions
Yes, you can cancel anytime from the Subscription tab in your account settings on the Perlego website. Your subscription will stay active until the end of your current billing period. Learn how to cancel your subscription
No, books cannot be downloaded as external files, such as PDFs, for use outside of Perlego. However, you can download books within the Perlego app for offline reading on mobile or tablet. Learn how to download books offline
Perlego offers two plans: Essential and Complete
- Essential is ideal for learners and professionals who enjoy exploring a wide range of subjects. Access the Essential Library with 800,000+ trusted titles and best-sellers across business, personal growth, and the humanities. Includes unlimited reading time and Standard Read Aloud voice.
- Complete: Perfect for advanced learners and researchers needing full, unrestricted access. Unlock 1.5M+ books across hundreds of subjects, including academic and specialized titles. The Complete Plan also includes advanced features like Premium Read Aloud and Research Assistant.
We are an online textbook subscription service, where you can get access to an entire online library for less than the price of a single book per month. With over 1.5 million books across 990+ topics, we’ve got you covered! Learn about our mission
Look out for the read-aloud symbol on your next book to see if you can listen to it. The read-aloud tool reads text aloud for you, highlighting the text as it is being read. You can pause it, speed it up and slow it down. Learn more about Read Aloud
Yes! You can use the Perlego app on both iOS and Android devices to read anytime, anywhere — even offline. Perfect for commutes or when you’re on the go.
Please note we cannot support devices running on iOS 13 and Android 7 or earlier. Learn more about using the app
Please note we cannot support devices running on iOS 13 and Android 7 or earlier. Learn more about using the app
Yes, you can access Farmacoeconomia by Fabrizio Gianfrate in PDF and/or ePUB format, as well as other popular books in Business & Pharmaceutical, Biotechnology & Healthcare Industry. We have over 1.5 million books available in our catalogue for you to explore.