
eBook - ePub
El origen de la vida
Juan Antonio Aguilera
This is a test
Share book
- 144 pages
- Spanish
- ePUB (mobile friendly)
- Available on iOS & Android
eBook - ePub
El origen de la vida
Juan Antonio Aguilera
Book details
Book preview
Table of contents
Citations
About This Book
A lo largo de la historia, todas las culturas han desarrollado teorías que tratan de explicar la aparición de los primeros organismos en nuestro planeta. En los últimos años, los avances en biología y genética han abierto nuevas posibilidades. ¿Es posible descubrir nuestro origen? ¿Llegaremos a recrear la vida de manera controlada en un laboratorio? ¿Existe vida en otros lugares del universo? Recorrer el camino hacia el pasado es, al mismo tiempo, una mirada al futuro.
Frequently asked questions
How do I cancel my subscription?
Can/how do I download books?
At the moment all of our mobile-responsive ePub books are available to download via the app. Most of our PDFs are also available to download and we're working on making the final remaining ones downloadable now. Learn more here.
What is the difference between the pricing plans?
Both plans give you full access to the library and all of Perlego’s features. The only differences are the price and subscription period: With the annual plan you’ll save around 30% compared to 12 months on the monthly plan.
What is Perlego?
We are an online textbook subscription service, where you can get access to an entire online library for less than the price of a single book per month. With over 1 million books across 1000+ topics, we’ve got you covered! Learn more here.
Do you support text-to-speech?
Look out for the read-aloud symbol on your next book to see if you can listen to it. The read-aloud tool reads text aloud for you, highlighting the text as it is being read. You can pause it, speed it up and slow it down. Learn more here.
Is El origen de la vida an online PDF/ePUB?
Yes, you can access El origen de la vida by Juan Antonio Aguilera in PDF and/or ePUB format, as well as other popular books in Medicina & Microbiología y parasitología médicas. We have over one million books available in our catalogue for you to explore.
Information
Topic
MedicinaLa génesis de las primeras células
Recordemos las tres características esenciales e interrelacionadas de los seres vivos: una base genética para la replicación de la información, un metabolismo para las relaciones y el automantenimiento, y una celularidad mediada por membranas que, acoplada con las otras dos propiedades, permite el juego evolutivo basado en la reproducción con variaciones. El hallazgo del ARN catalítico alentó las expectativas de que este ácido nucleico diera cuenta al menos de las dos primeras, pero es necesario explicar cómo pudo aparecer en la Tierra primitiva.
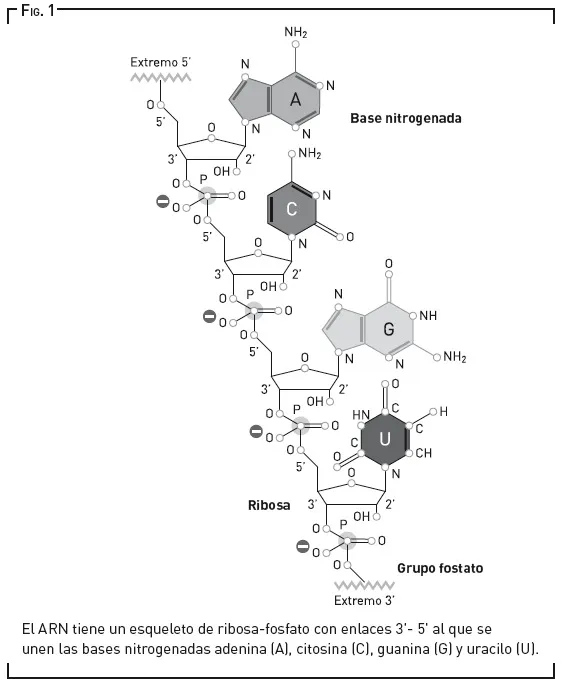
Aunque aceptemos la presencia de bases nitrogenadas en la Tierra prebiótica, avanzar un paso más y sintetizar un ribonucleótido, la unidad fundamental del ARN, es difícil. Los intentos de conseguir las uniones de sus tres componentes —ribosa, fosfato y base nitrogenada, como se ve en la figura 1— con un rendimiento aceptable en condiciones prebióticas han fracasado una y otra vez. Además, una vez que se tienen los nucleótidos, hay que engarzarlos mediante reacciones químicas en las que se produce agua. Y, aunque solemos asociarla con la vida, hay momentos en los que el agua estorba.
LA DIFÍCIL REPLICACIÓN ESPONTÁNEA DEL ARN
Para que exista un mundo del ARN no es suficiente que haya ARN. Este, además, debe poder replicarse con una conservación aceptable de su secuencia de bases, que es donde se almacena la información genética que debe transmitirse.
Desde hace años se está persiguiendo replicar el ARN en ausencia de enzimas proteicas de dos maneras: sin actividad enzimática alguna, o con la de los propios ARN. Para conseguir replicar ARN sin enzimas de ningún tipo, se parte de unos ARN iniciales y de nucleótidos o derivados de estos. El químico británico Leslie Orgel trabajó durante décadas en este sentido y, tras algunos logros parciales, acabó por tirar la toalla. Otros investigadores la han recogido y han conseguido cadenas de varias decenas de nucleótidos, pero en condiciones poco verosímiles como prebióticas.
Entre quienes utilizan las actividades enzimáticas de los ARN destacan el nobel de Medicina Jack Szostak (en la fotografía inferior derecha de la página 83) y Gerald Joyce, que lleva más de dos décadas intentando, conseguir una ARN replicasa, un ARN capaz de catalizar su propia replicación. En 2014 ya hablaba de un «superreplicador» eficientísimo, pero funcionaba bajo unos supuestos muy improbables en la Tierra primordial. El químico español Carlos Briones y sus colaboradores postulan un mecanismo más plausible para obtener secuencias largas: mediante la unión de trozos cortos de ARN que podrían exhibir la actividad ligasa necesaria para llevar a cabo las reacciones que dan lugar a la unión de las moléculas. El proceso tendría lugar sobre la superficie de arcillas o en el interior de vesículas.
En todo caso, es muy discutible el interés de unas ARN replicasas o ligasas solas ante el peligro de un medio acuoso prebiótico. Sin nada que los proteja, los ARN tienen una aciaga tendencia a descomponerse por la acción del agua, una reacción que se conoce como hidrólisis. El balance a finales del siglo XX era desolador, pues no se vislumbraba una manera creíble de formar los ARN necesarios para el mundo del ARN.
Es ingenuo pensar en unos ARN prebióticos sin una red de reacciones que los fabricaran y sustentaran. Por eso, diversos autores ya no confían en un mundo de ARN «limpio», sin apenas otros compuestos de interés probiótico. Cada vez se extiende más la idea de que la clave pudo estar en la cooperación molecular, y de que esta pudo darse desde mucho antes de la aparición del ARN.
No son pocos los expertos que piensan que a los ARN debieron precederlos unos polímeros con capacidades parecidas pero de formación mucho más sencilla en la Tierra prebiótica. Stanley Miller declaró que «todo el que esté buscando el esqueleto de ribosa-fosfato está errando el tiro». El principal problema está en la ribosa, por lo que se está buscando un pre-ARN de tipo AXN que sí se forme en ambientes prebióticos, y que pudiera dar paso a los ARN a través de moléculas intermedias AXN-ARN.
UN METABOLISMO ANTERIOR A LA VIDA
Algunos científicos, ante las dificultades para construir nucleótidos en condiciones prebióticas, y más aún ARN que se repliquen, no ven otra salida que la de generar primero una complejidad química que no consistiría simplemente en una suma de posibles precursores. También hay unas necesidades energéticas, pues la síntesis y el mantenimiento de los ARN tienen un alto coste en este sentido.
Se requeriría una serie de compuestos que formaran redes autosostenidas de reacciones químicas, a semejanza de las que vemos en el metabolismo de todos los seres vivos actuales. Ese autosostenimiento se basa en la autocatálisis. Se habla de autocatálisis cuando un compuesto promueve su propia formación (1X→2X); en realidad, el ARN replicador que mencionábamos antes supone una manera de conseguir una autocatálisis (1ARN→2ARN); también hay autocatálisis en el caso de la hipótesis que propugna que el ARN favorecería la formación de péptidos que promovieran la síntesis de ARN. La autocatálisis, según demostró el químico belga Ilya Prigogine, es clave en los procesos de autoorganización. Como señala el estadounidense Stuart Kauffman, uno de los biólogos teóricos más relevantes en el ámbito de la complejidad biológica, cuando se reproducen los seres vivos actuales es autocatalítico todo el conjunto, pues no cabe hablar de la reproducción aislada del ADN, de la membrana…
LOS AXN COMO PRECURSORES DEL ARN
En los llamados AXN, la X sustituye a la ribosa (R), el azúcar que, alternado con fosfato, conforma el «esqueleto» de los ARN. Se han propuesto diversos candidatos para la «X», y con algunos, sobre todo con el glicerol (con tres átomos de carbono) y la treosa (con cuatro), se han conseguido resultados preliminares prometedores de cara a la obtención de cadenas de «AGN» o «ATN». La treosa es un azúcar no quiral de menor tamaño que la ribosa y más abundante en los meteoritos. Con ella se han llegado a obtener incluso cadenas dobles ATN/ATN, así como híbridos ATN/ARN, y se especula con un «mundo del ATN» que podría haber facilitado la llegada del ARN. Diversos AXN han mostrado actividades catalíticas que ayudan a imaginar esos «mundos» activos.
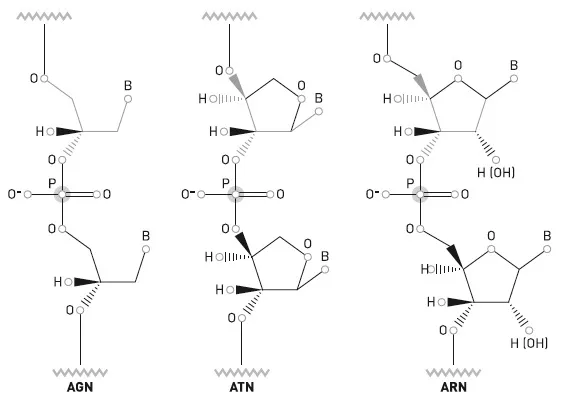
Comparación de las estructuras de dos candidatos a pre-ARN (AGN y ATN) con la del ARN. La letra B representa las bases nitrogenadas.
En definitiva, nos interesa encontrar un metabolismo con reacciones, rutas, ciclos o redes autocatalíticas. Y, antes o después, todo ello hay que empaparlo de control, como el que se ejerce con las realimentaciones negativas, que impiden que las positivas — de tipo autocatalítico— se desboquen. La vida se basa en un equilibrio dinámico entre los controles negativos y la autocatálisis y entre la cooperación y la competición a muy distintos niveles.
¿Es posible que sin enzimas se genere una red semejante a la metabólica? Y, sobre todo, ¿es posible que una red así evolucione? Kauffman defiende que sí, que cuando una diversidad de compuestos químicos alcanza una densidad y un tamaño críticos, se autoorganiza formando una red compleja capaz de evolucionar. Pero en este momento queremos algo más concreto y tangible, de modo que nos adentraremos en la propuesta de «metabolismo primero» más elaborada y debatida.
UNA CUNA DE PIRITA EN LAS PROFUNDIDADES MARINAS
En 1988, una nueva hipótesis sacudió a la comunidad científica del origen de la vida. La lanzó Günter Wächtershäuser (en la fotografía inferior izquierda de la página contigua), un químico alemán a la sazón desconocido que trabajaba, como Einstein en su tiempo, en una empresa de patentes, en este caso en Múnich. Esos datos biográficos, al evocar los del gran físico, llevaron a Gerald Joyce —uno de sus críticos— a decir con cierta chanza: «Dado el precedente, sospecho que lo mejor que podríamos hacer es tomarlo en serio».


Arriba, fumarolas submarinas, el escenario en el que, según G. Wächtershäuser (abajo a la izquierda), surgió la primera característica de la vida: el metabolismo. Otros autores, como J. Szostak (abajo a la derecha), sostienen que genética, metabolismo y compartimentación se originaron de forma simultánea.
El autor propuso que los organismos pioneros fueron muy diferentes de los que conocemos, pues carecerían de membranas y de enzimas, pero sí exhibirían un metabolismo. Los metabolitos se localizarían sobre una superficie, de modo que se habla de organismos bidimensionales (e, informalmente, de pizza en vez de sopa). No dispondrían de ácidos nucleicos ni de otras moléculas portadoras de información. No obstante, habría herencia, selección y, en definitiva, capacidad de evolución.
Todos estos metabolitos tendrían cargas negativas, como la mayoría de los actuales, y estarían unidos por atracción electrostática a superficies de pirita, con cargas positivas, en un medio acuoso caliente y ácido. Como la pirita es un sulfuro de hierro (FeS2), se habla de un «mundo del hierro-azufre». El escenario que encaja con esta hipótesis es el de las chimeneas hidrotermales conocidas como fumarolas negras, en los fondos oceánicos (véase la fotografía superior de la página anterior), donde en la actualidad prosperan complejos ecosistemas. Todos los compuestos orgánicos se formarían in situ, de modo que estaríamos ante un metabolismo que se autoabastece, lo que se denomina autotrófico. Este «metabolismo de superficie» se extendería mediante más reacciones químicas. ¿Qué impulsaría estas reacciones? La energía y el poder reductor necesarios provendrían de la reacción de formación de pirita.
Pero eso es solo el comienzo. Wächtershäuser planteó una detallada serie de reacciones que comienza con la asimilación del monóxido o dióxido de carbono y acaba con la generación de células «modernas». La gran ruta autocatalítica fijadora de CO2 fue, según el autor, una vieja conocida, la secuencia de reacciones que corresponde al ciclo de Krebs, pero funcionando al revés (fig. 2) y sin enzimas. El ciclo de Krebs avanza en muchas especies, como la nuestra, en un «sentido oxidante», de modo que las moléculas procedentes de la degradación de glúcidos, lípidos y proteínas se oxidan liberando dióxido de carbono y energía. Esa energía se almacena en forma de ATP (adenosín trifosfato), la ubicua molécula que sirve como «moneda de intercambio energético» de los seres vivos. El ciclo inverso, en cambio, promovería la reducción y fijaci...